L’Agenzia europea del farmaco ha avviato la valutazione della domanda presentata da Johnson & Johnson per l’uso di una dose di richiamo del suo vaccino anti-Covid sviluppato dalla divisione farmaceutica Janssen, da somministrare almeno 2 mesi dopo la prima dose a persone di età pari o superiore a 18 anni.
L’EMA spiega che “il Comitato per i medicinali a uso umano Chmp effettuerà una valutazione accelerata dei dati presentati dalla società“. Questi dati includono “i risultati su oltre 14mila adulti che hanno ricevuto una seconda dose di vaccino Covid Janssen o un placebo a 2 mesi di distanza dalla dose iniziale“.
Gli esperti valuteranno se gli aggiornamenti alle informazioni sul prodotto sono appropriati. L’esito di questa valutazione, informa l’EMA, è previsto entro settimane, a meno che non siano necessarie informazioni supplementari.
Il vaccino J&J, a vettore adenovirale, è attualmente autorizzato per l’uso in over 18 in versione “monodose“, cioè con vaccinazione primaria costituita da una singola iniezione.
L’EMA ha precisato che “l’attuazione delle campagne di vaccinazione nell’Ue, compreso l’uso dei richiami, rimane prerogativa dei gruppi consultivi tecnici nazionali sull’immunizzazione (Nitag) che guidano le campagne in ciascuno Stato membro. Questi organismi sono nella posizione migliore per tenere conto delle condizioni locali, compresa la diffusione del virus (in particolare qualsiasi variante di preoccupazione), la disponibilità di vaccini e le capacità dei sistemi sanitari nazionali“.
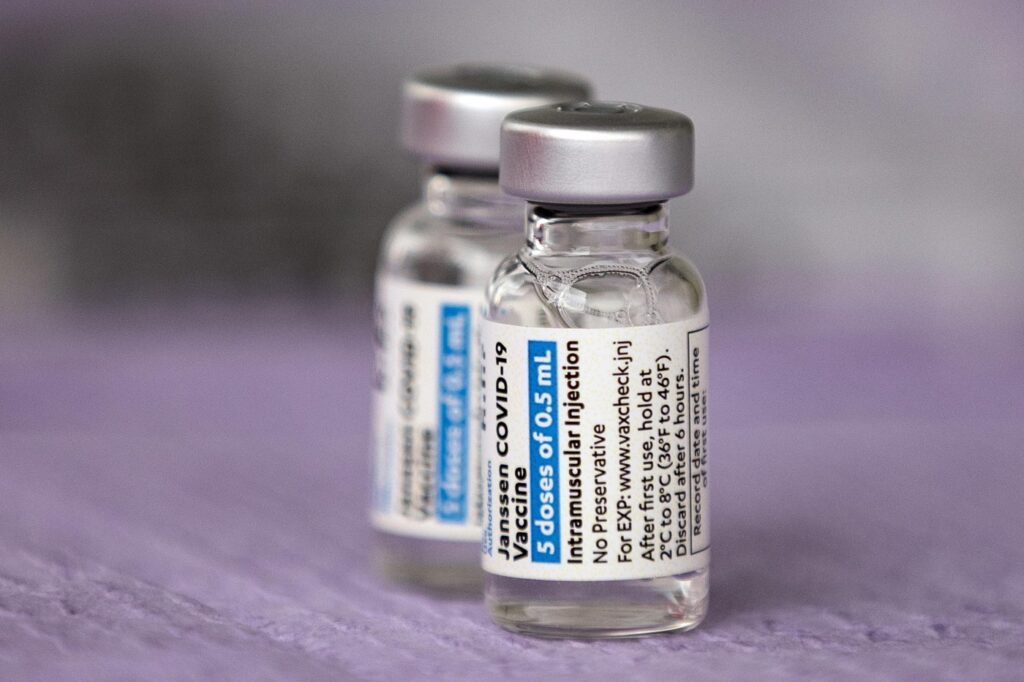
Covid, vaccino Johnson & Johnson: l’EMA avvia valutazione per la dose di richiamo
Il vaccino J&J, a vettore adenovirale, è attualmente autorizzato per l'uso in over 18 in versione "monodose"